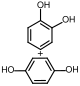
Υδροκινόνη 98% 250gr
Η υδροκινόνη (αγγλικά hydroquinone) είναι αρωματική οργανική ένωση, με μοριακό τύπο C6H6O2, αν και συχνά παριστάνεται πιο αναλυτικά, με τον ημισυντακτικό τύπο π-C6H4(OH)2. Αποτελεί την παρα-ισομερή, από τις τρεις (3) ισομερείς βενζο(λο)διόλες, δηλαδή στις διφαινόλες, που αποτελούν υποσύνολο των αρενοδιολών. Η χημικά καθαρή υδροκινόνη, στις κανονικές συνθήκες περιβάλλοντος, δηλαδή σε θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι κοκκώδες στερεό. Ο όρος «υδροκινόνη» αναφέρεται επίσης κατ’ επέκταση και σε ομάδα «θυγατρικών» παραγώγων ή και υποκατεστημένων ενώσεων.
Φυσικοχημικές Ιδιότητες
Μοριακός τύπος: C6H6O2
Μοριακό βάρος: 110.112 g·mol−1
Σημείο ζέσης: 287 °C
Σημείο τήξης: 172 °C
Πυκνότητα: 1.3 g cm−3
Εμφάνιση: άσπρο στερεό
Χημική δομή

Ασφάλεια και αποθήκευση



Προκαλεί ερεθισμό Διαβρωτικό Επικίνδυνο για την υγεία Επικίνδυνο για το περιβάλλον
στα μάτια και στο δέρμα
Αναλυτική Περιγραφή
Φυσική παρουσία
Οι υδροκινόνες είναι από τα κύρια συστατικά του αμυντικού υγρού του βομβαρδιστή (μιας κατηγορίας σκαθαριών), σε συνδυασμό με υπεροξείδιο του υδρογόνου (H2O2), ίσως και με άλλες ενώσεις, ανάλογα με το είδος, που παράγεται από αδένες και μερικά από τα συστατικά συλλέγονται σε ειδική κύστη. Η κύστη αυτή ανοιγοκλείνει μέσω μιας βαλβίδας που ελέγχεται από ειδικό μυ, και το περιεχόμενό της πηγαίνει σε ένα θάλαμο αντίδρασης, με (σχετικά) χονδρά τοιχώματα, που περιέχει ειδικά κύτταρα, τα οποία παράγουν καταλάσες και υπεροξειδάσες. Αυτές καταλύουν την οξείδωση των υδροκινοκών στις αντίστοιχες κινόνες. Οι αντιδράσεις αυτές απελευθερώνουν οξυγόνο και παράγουν αρκετή θερμότητα, ώστε το μείγμα να φθάσει στην κανονική θερμοκρασία βρασμού του και έτσι να εξαερωθεί το 1/5 της ποσότητάς του, δημιουργώντας έτσι ένα ζεστό αερόλυμα, με το οποίο το σκαθάρι ψεκάζει τους εχθρούς του, από ειδικό άνοιγμα στην κοιλιακή του χώρα.
Παράγωγα της φαρνεσυλυδροκινόνης αποτελούν τις κύριες ερεθιστικές ουσίες που αποπνέουν τα Eriodictyon parryi, οι οποίες μπορούν να προκαλέσουν σοβαρή δερματίτιδα, σε περίπτωση επαφής με το ανθρώπινο δέρμα.
Η υδροκινόνη θεωρείται ότι αποτελεί την ενεργή τοξίνη στα μανιτάρια agaricus hondensis.
Η υδροκινόνη έχει αποδειχθεί ότι είναι ένα από τα χημικά συστατικά των φυσικών προϊόντων πρόπολης.
Είναι επίσης μία από τις χημικές ενώσεις που βρίσκονται στο καστόριο. Αυτή η ένωση, μαζί με άλλες συλλέγονται από τις καστόριες κύστες των καστόρων .
Στην κουμαριά (arctostaphylos uva-ursi), η αρβουτίνη μετατρέπεται σε υδροκινόνη.
Παραγωγή
Η υδροκινόνη παράγεται βιομηχανικά από δύο κύριες παραγωγικές οδούς.
1. Η ευρύτερα χρησιμοποιούμενη παραγωγική οδός διαδρομή είναι παρόμοια με τη διεργασία κουμενίου, σε μηχανισμό αντίδρασης, και εμπλέκει διαλκυλίωση του βενζολίου με προπένιο, που δίνει 1,4-διισοπροπυλοβενζόλιο. Η τελευταία ένωση αντιδρά με το οξυγόνο του ατμοσφαιρικού αέρα, δίνοντας το αντίστοιχο διυδροϋπεροξείδιο, που δομικά είναι παρόμοιο με το υπεροξείδιο του κουμενίου, οπότε ομοίως με μετάθεση δίνει προπανόνη και υδροκινόνη, μετά από επίδραση οξέος.
2. Μια δεύτερη παραγωγική οδός εμπλέκει υδροξυλίωση φαινόλης. Η μετατροπή αυτή γίνεται με επίδραση υπεροξειδίου του υδρογόνου (H2O2), που παρέχει ένα μείγμα υδροκινόνης και κατεχόλης:
Άλλες, λιγότερο συνηθισμένες μέθοδοι συμπεριλαμβάνουν:
- Την οξείδωση της ανιλίνης από διοξείδιο του μαγγανίου (MnO2), που ακολουθείται από αναγωγή της προκύπτουσας 1,4-βενζοκινόνης. Η διαδικασία έχει ορισμένα σημαντικά μειονεκτήματα: διεξάγεται ασυνεχώς κατά ποσότητες υλικού και επιπλέον δημιουργεί σημαντική ροή αποβλήτων.
- Μια δυνητικά σημαντική μέθοδος σύνθεσης υδροκινόνης που έχει προταθεί χρησιμοποιεί αιθίνιο (HC≡CH) και πεντακαρβονυλοσίδηρο [Fe(CO)5]. Ο πεντακαρβονυλοσίδηρος λειτουργεί ως καταλύτης και όχι ως αντιδραστήριο, αν παρέχεται επιπλέον αέριο μονοξείδιο του άνθρακα (CO). Το ρόδιο ή το ρουθήνιο μπορούν να υποκαταστήσουν τον σίδηρο ως καταλύτες, με ευνοϊκές αποδόσεις, αλλά συνήθως δεν χρησιμοποιούνται λόγω του αυξημένου κόστους της αποκατάστασής τους στο αντιδρών μείγμα.
- Η υδροκινόνη και τα παράγωγά της μπορούν επίσης να παραχθούν με οξείδωση διάφορων φαινολών. Παραδείγματα περιλαμβάνουν τη μέθοδο της οξείδωσης με υπερθειικά κατά Ελμπς (Elbs persulfate) και τη μέθοδο της οξείδωση κατά Ντακίν.
Αντιδράσεις
Η πηγή δραστικότητα της υδροκινόνης είναι οι δύο (2) υδροξυλομάδες. Η δράση της μοιάζει με αυτήν των υπόλοιπων φαινολών, που είναι ασθενώς όξινες. Το αποτέλεσμα είναι οι συζυγείς βάσεις να επιδέχονται εύκολη O-αλκυλίωση, δίνοντας τους αντίστοιχους μονο- και δι- αιθέρες. Ομοίως, η υδροκινόνη είναι ιδιαίτερα επιρεπής σε διάφορες αντιδράσεις υποκατάστασης στο βενζολικό δακτύλιό της κατά Friedel-Crafts, όπως είναι αλκυλίωση. Αυτή η αντίδραση αξιοποιείται για την παραγωγή δημοφιλών αντιοξειδωτικών, όπως η 2-τριτ. βουτυλο-4-μεθοξυφαινόλη (BHA). Η χρήσιμη χρωστική κινιζαρίνη παράγεται με διακυλίωση της υδροκινόνης με φθαλικό ανυδρίτη.
Οξειδοαναγωγής
Η υδροκινόνη υφίσταται οξείδωση κάτω από ήπιες συνθήκες, δίνοντας ως προϊόν βενζοκινόνη. Αυτή η διαδικασία μπορεί να αντιστραφεί. Μερικά φυσικά παράγωγα της υδροκινόνης εμφανίζουν αυτό το είδος της αντιδραστικότητας, όπως για παράδειγμα το συνένζυμο Q. Η αντίδραση αξιοποιείται βιομηχανικά, τόσο με την ίδια την υδροκινόνη, όσο και με παράγωγά της
είναι η εκμετάλλευση και οι δύο με την υδροκινόνη ίδια, αλλά πιο συχνά με παράγωγά της, στα οποία το ένα (1) υδροξύλιο έχει αντικατασταθεί από αμινομάδα.
Αμίνωση
Μια σημαντική αντίδραση είναι η μετατροπή της υδροκινόνης σε μονο- και διαμινο-παράγωγα. Η μεθυλαμινοφαινόλη, που χρησιμοποιούνται στη φωτογραφία, παράγεται με τον εξής τρόπο:
- C6H4(Ω)2 + CH3NH2 → C6H4(Ω)(N(H)CH3) + H2O
Ομοίως, διαμίνες χρήσιμες στη βιομηχανία ελαστικών, όπως antiozone παράγοντες, παράγονται με παρόμοιο τρόπο από την ανιλίνη:
- C6H4(Ω)2 + 2 C6H5NH2 → C6H4(N(H)C6H5)2 + 2 H2O
Χρήσεις
Η υδροκινόνη έχει μια ποικιλία χρήσεων, κυρίως σχετικών με τη δράση της ως αναγωγικού παράγοντα που είναι διαλυτός στο νερό. Είναι ένα σημαντικό συστατικό στο πιο μαύρο και λευκό φωτογραφικό προγραμματιστές για την ταινία και το έγγραφο, όπου, με την ένωση metol, ανάγει τα αλογονίδια του αργύρου σε στοιχειακό άργυρο.
Υπάρχουν διάφορες άλλες χρήσεις που συνδέονται με τη μείωση της δύναμης. Ως αναστολέας πολυμερισμού, υδροκινόνη εμποδίζει τον πολυμερισμό της ακρυλικό οξύ, μεθακρυλικό μεθύλιο, κυανοακρυλική κόλλα, και άλλα μονομερή τα οποία είναι ευαίσθητα σε ριζοσπαστική-ξεκίνησε πολυμερισμού. Αυτή η εφαρμογή εκμεταλλεύεται τις αντιοξειδωτικές ιδιότητες της υδροκινόνης.
Η υδροκινόνη μπορεί να υποστεί ήπια οξείδωση για να μετατραπεί στο σύνθετο παραβενζοκινόνη, C6H4O2, που συχνά ονομάζεται p-κινόνη ή απλά κινόνη. Αναγωγή της κινόνης αντιστρέφει αυτή την αντίδραση προς υδροκινόνη. Ορισμένες βιοχημικές ενώσεις στη φύση έχουν αυτό το είδος της υδροκινόνης ή κινόνης τμήμα τους δομές, όπως το Συνένζυμο Q, και μπορεί να υποβληθεί σε παρόμοιες οξειδοαναγωγικές μετατροπές.
Η υδροκινόνη μπορεί να χάσει ένα η+ από τα δύο για να σχηματίσουν ένα diphenolate ιόντων. Το diνατρίου diphenolate αλάτι της υδροκινόνης χρησιμοποιείται ως ένα εναλλασσόμενο coμονομερούς μονάδας για την παραγωγή του πολυμερές PEEK.


 Φυσική
Φυσική Χημεία
Χημεία Βιολογία
Βιολογία Μαθηματικά
Μαθηματικά Περιβάλλον – Οικολογία
Περιβάλλον – Οικολογία Επιστήμες της Γης
Επιστήμες της Γης Τεχνολογία
Τεχνολογία Προσχολικά – Σχολικά
Προσχολικά – Σχολικά Ειδική Αγωγή
Ειδική Αγωγή Σχολικός Εξοπλισμός
Σχολικός Εξοπλισμός Τέχνες & Αθλητισμός
Τέχνες & Αθλητισμός Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική
Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική Ψηφιακή Τάξη
Ψηφιακή Τάξη Απαγωγοί
Απαγωγοί Ντουλάπες Φύλαξης
Ντουλάπες Φύλαξης Ψυγεία Καταψύκτες
Ψυγεία Καταψύκτες Εργαστηριακές Συσκευές
Εργαστηριακές Συσκευές Πάγιος Εργαστηριακός Εξοπλισμός
Πάγιος Εργαστηριακός Εξοπλισμός Χημικά Αντιδραστήρια
Χημικά Αντιδραστήρια Ιατρικός – Νοσοκομειακός εξοπλισμός
Ιατρικός – Νοσοκομειακός εξοπλισμός Μικροσκόπια – Στερεοσκόπια
Μικροσκόπια – Στερεοσκόπια USB Αισθητήρες & MBL Αισθητήρες
USB Αισθητήρες & MBL Αισθητήρες STEM EDUCATION
STEM EDUCATION Science School
Science School Εργαστήρια Δεξιοτήτων
Εργαστήρια Δεξιοτήτων Φυσικών Επιστημών Προσχολικής
Φυσικών Επιστημών Προσχολικής Φυσικών Επιστημών Ε & ΣΤ Δημοτικού
Φυσικών Επιστημών Ε & ΣΤ Δημοτικού Πακέτα Ασκήσεων Δευτεροβάθμιας
Πακέτα Ασκήσεων Δευτεροβάθμιας Η Φυσική με Πειράματα – Γυμνασίου
Η Φυσική με Πειράματα – Γυμνασίου Εκπαιδευτικά Σετ
Εκπαιδευτικά Σετ Εκπαιδευτικά Πακέτα Μικροκλίμακας
Εκπαιδευτικά Πακέτα Μικροκλίμακας BeeBot
BeeBot Botzees
Botzees EDISON
EDISON Gigo
Gigo Botley
Botley Spike
Spike Εξοπλισμός Υπουργείου
Εξοπλισμός Υπουργείου Εξοπλισμός Σχολείων 1821
Εξοπλισμός Σχολείων 1821 Arduino
Arduino MicroBit
MicroBit Raspberry Pi
Raspberry Pi Elecfreaks
Elecfreaks Keyestudio
Keyestudio Fischertechnik
Fischertechnik Grove Πλατφόρμα Ανάπτυξης
Grove Πλατφόρμα Ανάπτυξης DFRobot
DFRobot WaveShare
WaveShare Αισθητήρες
Αισθητήρες Μοτέρ και Ενεργοποιητές
Μοτέρ και Ενεργοποιητές 3D Printing
3D Printing Laser Engraver
Laser Engraver Προσφορές
Προσφορές Drones
Drones