Επτάνιο 500ml
Το Επτάνιο είναι ένα αλκάνιο, δηλαδή άκυκλος κορεσμένος υδρογονάνθρακας, μοριακό τύπο C7H16 και ημισυντακτικό τύπο CH3(CH2)5CH3. Το επτάνιο έχει εξ’ ορισμού βαθμό οκτανίου μηδέν (0).
Ονοματολογία
Η ονομασία «επτάνιο» προέρχεται από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το πρόθεμα «επτ-» δηλώνει την παρουσία επτά (7) ατόμων άνθρακα ανά μόριο της ένωσης, το ενδιάμεσο «-αν-» δείχνει την παρουσία μόνο απλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-ιο» φανερώνει ότι δεν περιέχει χαρακτηριστικές ομάδες, δηλαδή ότι είναι υδρογονάνθρακας.
Δομή
Το μόριό του αποτελείται από επτά (7) άτομα άνθρακα (δύο (2) πρωτοταγή και πέντε (5) δευτεροταγή) και δεκαέξι (16) άτομα υδρογόνου.
Φυσικές ιδιότητες και ισομερή
Το επτάνιο έχει τα ακόλουθα οκτώ (8) [δέκα (10) αν μετρηθούν και τα εναντιομερή] ισομερή:
- CH3(CH2)3CH(CH3)2: 2-μεθυλεξάνιο ή ισοεπτάνιο.
- CH3(CH2)2*CH(CH3)CH2CH3: R,S-3-μεθυλεξάνιο.
- (CH3)3C(CH2)2CH3: 2,2-διμεθυλοπεντάνιο ή νεοεπτάνιο.
- (CH3)2CΗ*CH(CH3)CH2CH3: R,S-2,3-διμεθυλοπεντάνιο.
- (CH3)2CΗCH2CΗ(CH3)2: 2,4-διμεθυλοπεντάνιο.
- (CH3CH2)2C(CH3)2: 3,3-διμεθυλοπεντάνιο.
- (CH3CH2)3CH: αιθυλοπεντάνιο.
- (CH3)3CCH(CH3)2: τριμεθυλοβουτάνιο ή τριπτάνιο.
Τα ισομερή αυτά παρόλο που έχουν ίδιο χημικό τύπο και μοριακό βάρος, έχουν διαφορετικές δομές και διαφορετικές ιδιότητες.
| Συντακτικός τύπος Δομή | Όνομα IUPAC (ελληνική μορφή) Όνομα | Μοριακό Βάρος | Σημείο ζέσεως (°C, 1 atm) |
| κ-επτάνιο επτάνιο | 100,21 | 98,42 | |
| 2-μεθυλεξάνιο ισοεπτάνιο | 100,21 | 90 | |
| 3-μεθυλεξάνιο | 100,21 | 90,7 | |
| 2,2-διμεθυλοπεντάνιο νεοεπτάνιο | 100,21 | 77,9 | |
| 2,3-διμεθυλοπεντάνιο | 100,21 | 89,4 | |
| 2,4-διμεθυλοπεντάνιο | 100,21 | 80,5 | |
| 3,3-διμεθυλοπεντάνιο | 100,21 | 85,7 | |
 | αιθυλοπεντάνιο | 100,21 | 93,5 |
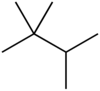 | τριμεθυλοβουτάνιο τριπτάνιο | 100,21 | 81,7 |
Χημικές ιδιότητες
Οξείδωση
1. Όπως όλα τα αλκάνια, το n-επτάνιο με περίσσεια οξυγόνου καίγεται προς διοξείδιο του άνθρακα και νερό:
{\displaystyle \mathrm {C_{7}H_{16}+11O_{2}{\xrightarrow {\triangle }}7CO_{2}+8H_{2}O+4828,44J} }
- Αν και η αντίδραση είναι μια έντονα εξώθερμη δεν συμβαίνει σε μέτριες θερμοκρασίες, γιατί για την έναρξή της πρέπει να υπερπηδηθεί πρώτα το εμπόδιο της διάσπασης των δεσμών C-C, των δεσμών C-H και των δεσμών (Ο=Ο) του O2:
2. Παραγωγή υδραερίου:
{\displaystyle \mathrm {C_{7}H_{16}+7H_{2}O{\xrightarrow[{700-1100^{o}C}]{Ni}}7CO+15H_{2}} }
3. Καταλυτική οξείδωση προς επτανάνη-2, επτανάνη-3 και επτανάνη-4:
{\displaystyle \mathrm {C_{7}H_{16}+O_{2}{\xrightarrow[{\triangle }]{Cu}}{\frac {2}{5}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}COCH_{3}+{\frac {2}{5}}CH_{3}CH_{2}CH_{2}CH_{2}COCH_{2}CH_{3}+{\frac {1}{5}}CH_{3}CH_{2}CH_{2}COCH_{2}CH_{2}CH_{3}+H_{2}O} }
- Είναι τα κύρια προϊόντα της καταλυτικής οξείδωσης του πεντανίου, αλλά παράγεται και μια μικρή ποσότητα επτανάλης.
Αλογόνωση
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{3}+X_{2}{\xrightarrow[{\triangle }]{UV}}aCH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}X+bCH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CHXCH_{3}+cCH_{3}CH_{2}CH_{2}CH_{2}CHXCH_{2}CH_{3}+dCH_{3}CH_{2}CH_{2}CHXCH_{2}CH_{2}CH_{3}+HX} }
- Δραστικότητα των X2: F2 > Cl2 > Br2 > Ι2.
- όπου 0<a,b,c,d<1, a + b + c + d = 0, διαφέρουν ανάλογα με το αλογόνο:
- Τα F και Cl είναι πιο δραστικά και λιγότερο εκλεκτικά. Η αναλογία των προπυλαλογονιδίων τους εξαρτάται κυρίως πό τη στατιστική αναλογία των προς αντικατάσταση ατόμων H. Ειδικά γοα το χλώριο θα έχουμε:
- 1-χλωρεπτάνιο: 6·1 = 6.
- 2-χλωρεπτάνιο: 4·3,8 = 15,2.
- 3-χλωρεπτάνιο: 4·3,8 = 15,2.
- 4-χλωρεπτάνιο: 2·3,8 = 7,6.
- Δηλαδή το μίγμα που προκύπτει είναι: 13,7% 1-χλωρεπτάνιο, 34,5% 2-χλωρεπτάνιο, 34,5% 3-χλωρεπτάνιο και 17,3% 4-χλωρεπτάνιο.
- Τα Br και I είναι πιο εκλεκτικά και λιγότερο δραστικά. Η αναλογία των πεντυλαλογονιδίων μεταβάλλεται προς όφελος των δευτεροταγών (αυτών που το αλογόνο συνδέεται με δευτεροταγές άτομο C, δηλαδή ατόμου C ενωμένου με 2 άλλα άτομα C) πεντυλοαλογονίδιων. Ειδικα για το βρώμιο θα έχουμε:
- 1-βρωμεπτάνιο: 6·1 = 6.
- 2-βρωμεπτάνιο: 4·82 = 328.
- 3-βρωμεπτάνιο: 4·82 = 328.
- 4-βρωμεπτάνιο: 2·82 = 162.
- Δηλαδή το μίγμα που προκύπτει είναι: 0,7% 1-βρωμεπτάνιο, 39,8% 2-βρωμεπτάνιο, 39,8% 3-βρωμεπτάνιο και 32,7% 4-βρωμεπτάνιο.
- Ανάλυση του μηχανισμού της χλωρίωσης του CH3(CH2)5CH3:
- 1. Έναρξη: Παράγονται ελεύθερες ρίζες.
{\displaystyle \mathrm {Cl_{2}{\xrightarrow[{\triangle }]{UV}}2Cl^{\bullet }-239kJ} }
- Η απαιτούμενη ενέργεια προέρχεται από το υπεριώδες φως (UV) ή θερμότητα (Δ).
- 2. Διάδοση: Καταναλώνονται οι παλιές ελεύθερες ρίζες, σχηματίζοντας νέες.
{\displaystyle \mathrm {CH_{3}(CH_{2})_{5}CH_{3}+Cl^{\bullet }{\xrightarrow {}}0,14CH_{3}(CH_{2})_{5}CH_{2}^{\bullet }+0,35CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{3}+0,35CH_{3}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{3}+0,35CH_{3}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{2}CH_{3}+HCl+14kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{3}+Cl_{2}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CHClCH_{3}+Cl^{\bullet }+100kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{3}+Cl_{2}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CHClCH_{2}CH_{3}+Cl^{\bullet }+100kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{2}CH_{3}+Cl_{2}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CHClCH_{2}CH_{2}CH_{3}+Cl^{\bullet }+100kJ} }
- 3. Τερματισμός: Καταναλώνονται μεταξύ τους οι ελεύθερες ρίζες, κατά τη στατιστικά σπάνια περίπτωση της συνάντησής τους.
{\displaystyle \mathrm {2Cl^{\bullet }{\xrightarrow {}}Cl_{2}+239kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}^{\bullet }+Cl^{\bullet }{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}Cl+339kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{3}+Cl^{\bullet }{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CHClCH_{3}+339kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{3}+Cl^{\bullet }{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CHClCH_{2}CH_{3}+339kJ} }
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{2}CH_{3}+Cl^{\bullet }{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CHClCH_{2}CH_{2}CH_{3}+339kJ} }
{\displaystyle \mathrm {2CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}^{\bullet }{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{3}+347kJ} }
{\displaystyle \mathrm {2CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{3}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH(CH_{3})CH(CH_{3})CH_{2}CH_{2}CH_{2}CH_{2}CH_{3}+347kJ} }
{\displaystyle \mathrm {2CH_{3}CH_{2}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{3}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH(CH_{2}CH_{3})CH(CH_{2}CH_{3})CH_{2}CH_{2}CH_{2}CH_{3}+347kJ} }
{\displaystyle \mathrm {2CH_{3}CH_{2}CH_{2}CH^{\bullet }CH_{2}CH_{2}CH_{3}{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH(CH_{2}CH_{2}CH_{3})CH(CH_{2}CH_{2}CH_{3})CH_{2}CH_{2}CH_{3}+347kJ} }
- Είναι όμως πρακτικά δύσκολο να σταματήσει η αντίδραση στην παραγωγή μονοαλογονοπαραγώγων.
- Αν χρησιμοποιηθούν ισομοριακές ποσότητες CH3(CH2)5CH3 και Χ2 θα παραχθεί μίγμα όλων των X-παραγώγων του CH3(CH2)5CH3
- Αν όμως χρησιμοποιηθει περίσσεια CH3(CH2)5CH3, τότε η απόδοση τωμ μονοπαραγώγων αυξάνεται πολύ, λόγω της αύξησης της στατιστική πιθανότητας συνάντισης CH3(CH2)5CH3 με X. σε σχέση με την πιθανότητα συνάντισης μονοπαραγώγου και X., που μπορεί να οδηγήσει στην παραγωγή των υπόλοιπων X-παραγώγων.
Παρεμβολή καρβενίων
- Τα καρβένια (π.χ. [:CH2]) μπορούν παρεμβληθούν στους δεσμούς C-H. Π.χ. έχουμε:
{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{3}+CH_{3}Cl+KOH{\xrightarrow {}}{\frac {3}{8}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{2}CH_{3}+{\frac {1}{4}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}CH(CH_{3})_{2}+{\frac {1}{4}}CH_{3}CH_{2}CH_{2}CH_{2}CH(CH_{3})CH_{2}CH_{3}+{\frac {1}{8}}CH_{3}CH_{2}CH_{2}CH(CH_{3})CH_{2}CH_{2}CH_{3}+KCl+H_{2}O} }
- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε;
- Παρεμβολή στους έξι (6) δεσμούς CH2-H: 6
- Παρεμβολή στους τέσσερεις (4) δεσμούς 2-CH-H: 4
- Παρεμβολή στους τέσσερεις (4) δεσμούς 3-CH-H: 4
- Παρεμβολή στους δύο (2) δεσμούς 4-CH-H: 2
Προκύπτει επομένως μίγμα οκτανίου ~37,5%, 2-μεθυλοεπτανίου ~25%, 3-μεθυλοεπτάνιου ~25% και 4-μεθυλοεπτάνιου 12,5%.
Καταλυτική ισομερείωση
Το επτάνιο μπορεί να υποστεί καταλυτική ισομερείωση προς όλα τα ισομερή του:
{\displaystyle \mathrm {CH_{3}(CH_{2})_{5}CH_{3}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}CH_{3}(CH_{2})_{4}CH(CH_{3})_{2}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}CH_{3}(CH_{2})_{3}CH(CH_{3})CH_{2}CH_{3}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}CH_{3}(CH_{2})_{2}CH(CH_{3})(CH_{2})_{2}CH_{3}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}} }
{\displaystyle \mathrm {(CH_{3})_{3}C(CH_{2})_{2}CH_{3}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}(CH_{3})_{2}CHCH(CH_{3})CH_{2}CH_{3}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}} }
{\displaystyle \mathrm {(CH_{3})_{2}CHCH_{2}CH(CH_{3})CH_{3}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}(CH_{3}CH_{2})_{2}C(CH_{3})_{2}{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}(CH_{3}CH_{2})_{3}CH{\stackrel {AlCl_{3}}{\overrightarrow {\longleftarrow }}}(CH_{3})_{3}CCH(CH_{3})_{2}} }


 Φυσική
Φυσική Χημεία
Χημεία Βιολογία
Βιολογία Μαθηματικά
Μαθηματικά Περιβάλλον – Οικολογία
Περιβάλλον – Οικολογία Επιστήμες της Γης
Επιστήμες της Γης Τεχνολογία
Τεχνολογία Προσχολικά – Σχολικά
Προσχολικά – Σχολικά Ειδική Αγωγή
Ειδική Αγωγή Σχολικός Εξοπλισμός
Σχολικός Εξοπλισμός Τέχνες & Αθλητισμός
Τέχνες & Αθλητισμός Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική
Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική Ψηφιακή Τάξη
Ψηφιακή Τάξη Απαγωγοί
Απαγωγοί Ντουλάπες Φύλαξης
Ντουλάπες Φύλαξης Ψυγεία Καταψύκτες
Ψυγεία Καταψύκτες Εργαστηριακές Συσκευές
Εργαστηριακές Συσκευές Πάγιος Εργαστηριακός Εξοπλισμός
Πάγιος Εργαστηριακός Εξοπλισμός Χημικά Αντιδραστήρια
Χημικά Αντιδραστήρια Ιατρικός – Νοσοκομειακός εξοπλισμός
Ιατρικός – Νοσοκομειακός εξοπλισμός Μικροσκόπια – Στερεοσκόπια
Μικροσκόπια – Στερεοσκόπια USB Αισθητήρες & MBL Αισθητήρες
USB Αισθητήρες & MBL Αισθητήρες STEM EDUCATION
STEM EDUCATION Science School
Science School Εργαστήρια Δεξιοτήτων
Εργαστήρια Δεξιοτήτων Φυσικών Επιστημών Προσχολικής
Φυσικών Επιστημών Προσχολικής Φυσικών Επιστημών Ε & ΣΤ Δημοτικού
Φυσικών Επιστημών Ε & ΣΤ Δημοτικού Πακέτα Ασκήσεων Δευτεροβάθμιας
Πακέτα Ασκήσεων Δευτεροβάθμιας Η Φυσική με Πειράματα – Γυμνασίου
Η Φυσική με Πειράματα – Γυμνασίου Εκπαιδευτικά Σετ
Εκπαιδευτικά Σετ Εκπαιδευτικά Πακέτα Μικροκλίμακας
Εκπαιδευτικά Πακέτα Μικροκλίμακας BeeBot
BeeBot Botzees
Botzees EDISON
EDISON Gigo
Gigo Botley
Botley Spike
Spike Εξοπλισμός Υπουργείου
Εξοπλισμός Υπουργείου Εξοπλισμός Σχολείων 1821
Εξοπλισμός Σχολείων 1821 Arduino
Arduino MicroBit
MicroBit Raspberry Pi
Raspberry Pi Elecfreaks
Elecfreaks Keyestudio
Keyestudio Fischertechnik
Fischertechnik Grove Πλατφόρμα Ανάπτυξης
Grove Πλατφόρμα Ανάπτυξης DFRobot
DFRobot WaveShare
WaveShare Αισθητήρες
Αισθητήρες Μοτέρ και Ενεργοποιητές
Μοτέρ και Ενεργοποιητές 3D Printing
3D Printing Laser Engraver
Laser Engraver Προσφορές
Προσφορές Drones
Drones